TEST REPORT PCR SHINEWAY

Analizzatore di acido nucleico per PCR (SWM01) e 2019-nCoV Kit di rilevamento dell’acido nucleico (SW-CoV-01)

1. Rapporto sulle prestazioni del prodotto
1.1 Presentazione del prodotto
1.1.1 Analizzatore di acido nucleico PCR SWM-01 L’analizzatore di acido nucleico PCR SWM-01 esegue il rilevamento qualitativo di campioni di acido nucleico (DNA/RNA) derivati dal corpo umano mediante PCR a fluorescenza singola, compresa la rilevazione di acido nucleico e l’analisi genica di agenti patogeni. Il prodotto può essere utilizzato in vari scenari tra cui CDC, cure mediche di emergenza, visita specialistica, cure primarie e screening del sangue. L’analizzatore di acido nucleico PCR SWM-01 è costituito dallo strumento e dall’alimentatore. Lo strumento è costituito da sistema di controllo, sistema di alimentazione, sistema fotoelettrico, sistema di controllo della temperatura, componente del case, chip di reazione, moduli software (incluso software di controllo, versione 1.0).
1.1.2 Kit di rilevamento dell’acido nucleico 2019-nCoV (SW-nCoV-01) Il reagente di rilevazione RT-PCR per il nuovo coronavirus è progettato sulla base delle regioni del gene ORF1ab e N fornite nella “Guida tecnica per il rilevamento di polmonite infetta da nuovo coronavirus”. Il kit impiega fluorofori FAM e ROX come acquisizione del segnale di fluorescenza, contenente l’enzima di rilevazione del virus RNA e il sistema buffer. 5 Il kit utilizza il metodo PCR con tecnologia di amplificazione della sonda fluorescente in grado di rilevare rapidamente il nuovo tipo di RNA del coronavirus (2019-nCoV) nel campione. La reazione viene eseguita continuamente nella stessa provetta, che è semplice da usare e può prevenire efficacemente la contaminazione.

1.2 Specifiche, modello e durata
1.2.1 Analizzatore di acido nucleico PCR SWM-01
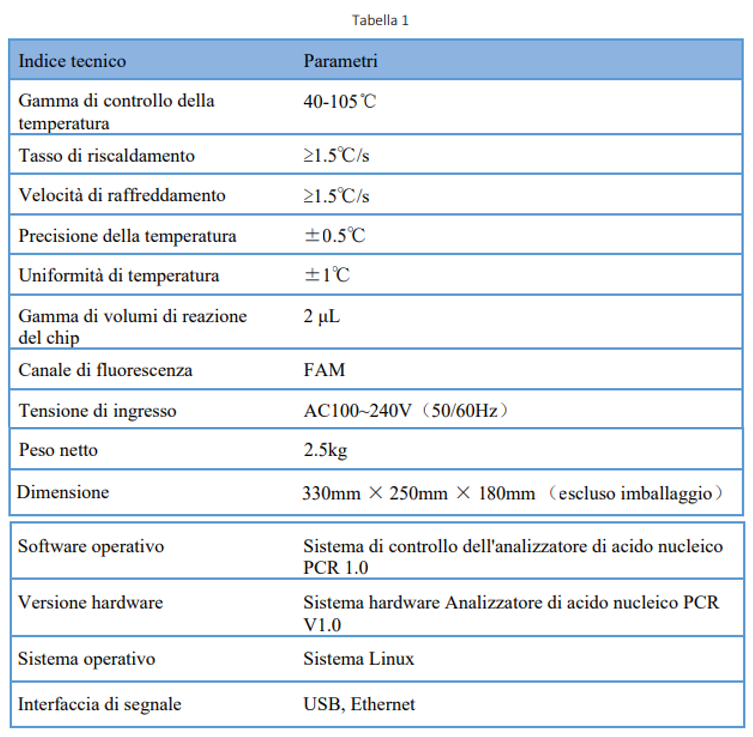
1.2.1.1 Modello: SWM-01
1.2.1.2 Versione: I
L’analizzatore di acido nucleico PCR SWM-01 non influisce negativamente sulla salute o sulla sicurezza dei pazienti, dell’utente e di altre persone durante la vita del prodotto.
1.2.2 Kit di rilevamento dell’acido nucleico 2019-nCoV (SW-nCoV-01)
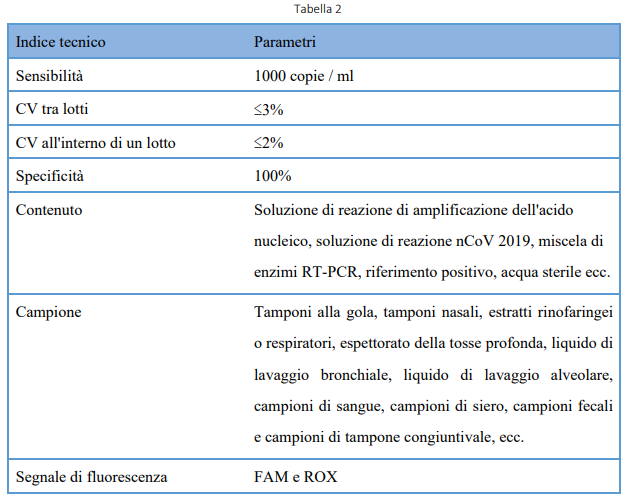
1.2.1.1 Modello: SW-nCoV-01
1.2.1.2 Versione I
1.2.2.3 Durata: 1 anno
Il kit di rilevamento dell’acido nucleico 2019-nCoV (SW-nCoV-01) non influisce negativamente sulla salute o sulla sicurezza dei pazienti, dell’utente e di altre persone durante la vita del prodotto
1.3 Meccanismo
Un micro-riscaldatore a pellicola sottile a base di silicio viene utilizzato come componente di riscaldamento rapido e un chip microfluidico viene utilizzato come supporto per la reazione PCR. Il sistema di reazione PCR utilizza una sonda fluorescente come indicazione del segnale di reazione. Man mano che la reazione della PCR progredisce, la fluorescenza della reazione positiva si accumula e il segnale viene raccolto come immagini da una telecamera CMOS. Infine, il sistema di controllo completa la raccolta dei dati ed effettua l’elaborazione delle immagini digitali.
1.3.1 Sistemi di controllo: sistemi di controllo integrati
1.3.2 Controllo della temperatura: basato sul principio del riscaldamento Joule, un microriscaldatore al silicio a pellicola sottile con rivestimento metallico viene utilizzato come elemento riscaldante, che ha un’alta conduttività termica e una buona curva lineare di resistenza alla temperatura, ottenendo così un aumento della temperatura rapido e preciso. Inoltre, il sistema di raffreddamento è dotato di una piccola ventola ad alta velocità e un condotto ottimizzato è stato progettato per aumentare efficacemente la velocità di raffreddamento.
1.3.3 Portatore di reazione: il chip microfluidico a base di silicio può essere utilizzato come supporto monouso per la reazione PCR. La camera di reazione interna ha un volume di 2 μL. Il substrato di silicio è strettamente a contatto con il micro-riscaldatore a pellicola sottile, che è utile per migliorare l’efficienza del trasferimento di calore e l’uniformità della temperatura. Coprire il substrato di silicio con un wafer di vetro per formare una camera di reazione PCR può efficacemente evitare la contaminazione del campione.
1.3.4 Rilevazione del segnale di fluorescenza: il sistema di reazione della PCR utilizza una sonda fluorescente o un colorante generale come indicazione del segnale. Man mano che la 9 reazione della PCR progredisce, la fluorescenza della reazione positiva si accumula e il segnale viene raccolto come immagini da una telecamera CMOS. Alla fine, il sistema di controllo completa la raccolta e l’elaborazione dei dati.
2 Studio delle prestazioni del prodotto
2.1 Esperimento di confronto tra reagente di riferimento e reagente sperimentale auto-progettato
1. Finalità
Il reagente sperimentale è il kit di rilevamento dell’acido nucleico HBV sviluppato indipendentemente dalla Shenzhen Shineway Technology Corporation. Analizzatore di acido nucleico per PCR SWM-01 deve essere utilizzato insieme al kit di rilevamento dell’acido nucleico (compatibilità ottimale). Il reagente di riferimento era il kit di rilevamento dell’acido nucleico HBV del gene Daan (tipo ipersensibile) dell’Università Sun Yat-sen, certificato dal CFDA (certificato nazionale di registrazione dello strumento 20173404069). Al fine di soddisfare la compatibilità tra il reagente di rilevazione e il tipo di macchina, il reagente sperimentale auto-sviluppato verrà utilizzato nel successivo test di verifica delle prestazioni dell’analizzatore di acido nucleico SWM-01 PCR. Pertanto, lo scopo di questo esperimento è verificare se il reagente sperimentale e il reagente di riferimento con certificazione CFDA hanno le stesse prestazioni di rilevamento quando utilizzato sullo strumento registrato, in modo da garantire l’efficacia del reagente sperimentale. Sono stati utilizzati campioni di siero clinico di HBV conservati nell’ottavo ospedale affiliato dell’Università di Sun Yat-sen (Shenzhen Futian District People’s Hospital) per testare il reagente di riferimento e il reagente sperimentale.
2. Materiali e strumenti
2.1Strumenti
Sistema LightCycler 480 per PCR in tempo reale, certificato di registrazione dello strumento nazionale per strumento di importazione 20163402935), mini centrifuga, micro pipetta, Tutti gli strumenti sopra indicati sono forniti dal laboratorio di medicina di laboratorio dell’ottavo ospedale affiliato, Università di Sun Yat-sen .
2.2 Materiali del kit di reagenti:
2.2.1 Kit di rilevamento dell’acido nucleico HBV del gene Daan (tipo ipersensibile) (certificato di registrazione dello strumento nazionale 20173404069 , Lotto n. 11 201903001) ;
2.2.2 Kit di rilevamento dell’acido nucleico HBV della Shenzhen Shineway Technology Corporation (lotto 201903001)
2.2.2 Kit di rilevamento dell’acido nucleico HBV della Shenzhen Shineway Technology Corporation (lotto numero 201812001)
2.3 Campioni I campioni di siero clinico HBV provenienti dall’ottavo ospedale affiliato dell’Università Sun Yat-sen sono stati estratti manualmente con il kit di estrazione di nutrienti a perline magnetiche Xi’an Tianlong. Il numero totale del campione è 95 e i campioni sono stati numerati da 1 a 95.
2.4 Kit di estrazione di nutrienti a perline magnetiche Xi’an Tianlong: Contiene tutti i materiali necessari per estrazione di acido nucleico.
2.5 Altri : chip di reazione, puntali di pipetta, guanti, maschere, banco (forniti dal laboratorio di medicina di laboratorio dell’ottavo ospedale affiliato, Università Sun Yat-sen).
3. Metodi
3.1Estrazione di acido nucleico
3.1.1 Aggiungere 25 µl di microsfere magnetiche (miscelate prima dell’uso), 20 µl di proteasi K, 500 µl di soluzione di lisato e 200 µl di campioni in una provetta da centrifuga senza enzimi da 1,5 ml e fare il bagno d’acqua a 60 ℃ per 15 minuti, mescolando più volte durante il bagno;
3.1.2 Posizionare la provetta da centrifuga sulla cremagliera magnetica per 3 minuti per attirare le microsfere magnetiche nella provetta, quindi rimuovere il liquido nella provetta e rimuovere la provetta da centrifuga
3.1.3 Aggiungere 700 µl di tampone di lavaggio A per far sospendere le microsfere magnetiche. Utilizzare il rack magnetico per attrarre le perle magnetiche per 3 minuti, quindi rimuovere il liquido nella provetta. Tenere la provetta da centrifuga sulla griglia magnetica;
3.1.4 Aggiungere 700 µl di tampone di lavaggio B, cercare di non soffiare via le microsfere magnetiche. Utilizzare la griglia magnetica per attirare le perle magnetiche e rimuovere il liquido nella provetta dopo 3 minuti, quindi rimuovere la provetta centrifuga;
3.1.5 Aggiungere 50 µl ~ 100 µl di tampone di eluizione, in modo tale da sospendere le sfere magnetiche. Fare un bagno d’acqua di 65 ℃ per 5 minuti, durante il quale agitare delicatamente la provetta per far eluire l’acido nucleico dalle microsfere magnetiche;
3.1.6 Posizionare la provetta da centrifuga sulla cremagliera magnetica per 3 minuti per 13 attirare le microsfere magnetiche, quindi trasferire il liquido con acido nucleico in una nuova provetta da centrifuga senza nucleasi da 1,5 ml e conservarla a -20 °C. 3.2 Preparazione del reagente di reazione 14
3.2.1 Estrarre il kit congelato, scongelarlo naturalmente a temperatura ambiente, mescolare delicatamente tutti i materiali reagenti nel kit e centrifugare a bassa velocità per un uso successivo.
3.2.2 Il metodo di preparazione del kit di rilevamento dell’acido nucleico HBV del gene Daan (tipo ipersensibile) è mostrato nella tabella seguente (preparare come guida per l’utente del kit di rilevamento)

3.2.3 Il metodo di preparazione del kit di rilevamento dell’acido nucleico di Shenzhen Shineway Technology Corporation HBV è mostrato nella tabella seguente
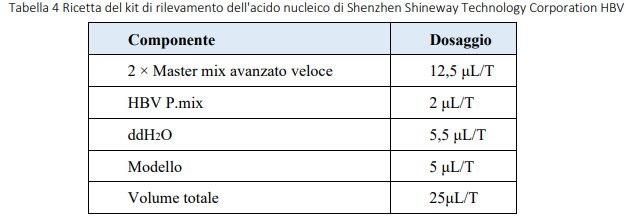
3.2.4Spiegazione I metodi di preparazione dei due kit HBV erano coerenti e sono stati rilevati campioni dal numero 1 al numero 95.
3.3Miscelazione del campione 5 μL di campione purificato estratto sono stati aggiunti a ciascuna soluzione di reazione.
3.4 Procedura di amplificazione della PCR – Kit di rilevamento dell’acido nucleico HBV del geneDaan:50 ℃ , 2 min ; 95 ℃ , 15 min ; (94 ℃ , 15 s ; 55 ℃ , 45 s) × 45 ciclo ; 40 ℃ , 20 S. 15 – Kit di rilevamento dell’acido nucleico HBV di Shenzhen Shineway Technology Corporation: 95 ℃ , 3 min ; (95 ℃ , 10 s ; 55 ℃ , 40 s) × 45 ciclo ; 40 ℃ , 20
3.5 Analisi dei dati 16 Il metodo di valutazione della coerenza KAPPA viene utilizzato per statistiche e analisi.
4. Risultati
4.1 Curva di amplificazione della fluorescenza
4.1.1 Risultati del numero di campione 1-95, utilizzando il kit di rilevamento dell’acido nucleico HBV del gene Daan (tipo ipersensibile):
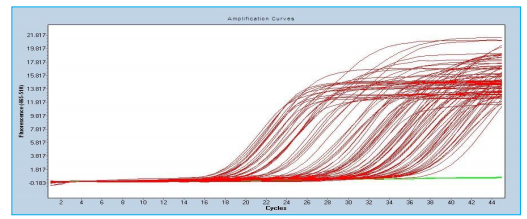
4.1.2 Risultati del numero di campione 1-95, utilizzando il kit di rilevamento dell’acido nucleico HBV di Shenzhen Shineway Technology Corporation:
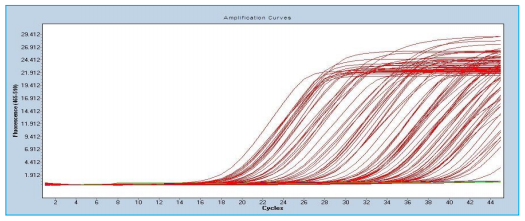
4.2 Valore Ct Confronto dei valori CT dei risultati di amplificazione tra reagente di riferimento e reagente sperimentale
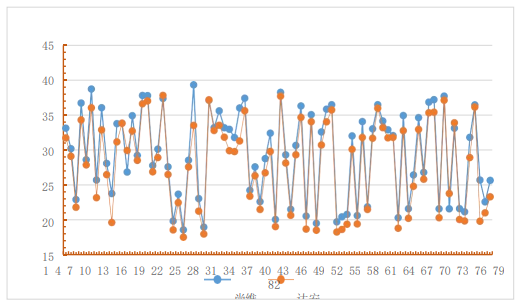
5. Analisi dei dati
Secondo i risultati del rilevamento di n. 1-95 campioni nell’ottavo ospedale affiliato dell’Università di Sun Yat-sen, non vi è alcuna differenza significativa tra i risultati di n. 1-95 campioni amplificati con kit del gene Daan e Shenzhen Shineway. Non vi è alcuna differenza tra i due reagenti nella determinazione di campioni negativi e positivi. Secondo l’analisi di consistenza del KAPPA, non vi è alcuna differenza tra il reagente sperimentale (kit di rilevamento dell’acido nucleico HBV della Shenzhen Shineway Technology Corporation) e il reagente di riferimento (kit di rilevamento dell’acido nucleico HBV del gene Daan). Secondo il metodo di test di coerenza KAPPA, la consistenza del reagente sperimentale e del reagente di riferimento è la più forte. A seguire:
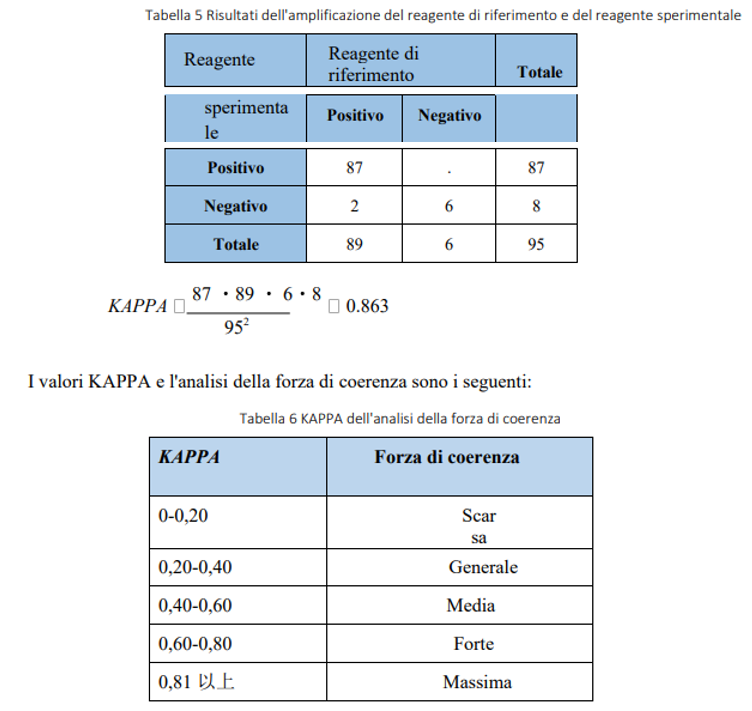
6. Conclusione
Sono stati condotti test di confronto tra il reagente di riferimento e il reagente sperimentale. L’analisi KAPPA di questi risultati ha mostrato che la forza di coerenza dei due kit era la più forte, indicando che non vi era alcuna differenza nell’effetto di amplificazione e nel giudizio positivo e negativo tra il reagente di riferimento e il reagente sperimentale.
2.2 Confronto delle prestazioni di SWM-01 con lo strumento commercializzato (campione Plasmid)
1. Finalità
Il frammento di plasmide HBV sintetico è stato usato come campione per confrontare la differenza di effetto di amplificazione e sensibilità tra l’analizzatore di acido nucleico PCM SWM-01 e il sistema di rilevamento PCR in tempo reale Bioer FQD-48A.
2. Materiali e strumenti
2.1 La sequenza del plasmide HBV è stata fornita dalla Shenzhen Shineway Technology Corporation e sintetizzata dalla GenScript Biotech Corporation;
2.2 Kit di rilevamento dell’acido nucleico HBV Shenzhen Shineway Technology Corporation (numero di lotto 201812001);
2.3 SWM-01 PCR Nucleic Acid Analyzer, il sistema di rilevamento PCR in tempo reale Bioer FQD- 48A (Certificato di registrazione dello strumento nazionale 20153400273) ;
2.4 Altri : chip di reazione, puntali di pipetta, guanti, maschere, banco (forniti dal laboratorio di medicina di laboratorio dell’ottavo ospedale affiliato, Università Sun Yat-sen).
3. Metodi
3.1 Estrarre il kit congelato, scongelarlo naturalmente a temperatura ambiente, mescolare delicatamente tutti i materiali reagenti e centrifugare a bassa velocità per un uso successivo.
3.2 Preparare diverse concentrazioni di campioni sintetici di plasmide HBV I plasmidi HBV sintetici sono stati conservati in provette EP, in uno stato di polvere, microscala (invisibile ad occhio nudo), la specifica è di 4 μg per provetta. Innanzitutto, tutti i materiali sono stati centrifugati a 12.000 RPM per 20 minuti, quindi sono stati aggiunti alla provetta 400 μL di 1 × soluzione di TE (pH = 8,09) per la dissoluzione del plasmide. Scorrere la provetta per 30 volte per miscelare l’omogeneità. I materiali sono stati centrifugati a 3000 RPM per un breve periodo. La concentrazione di plasmidi era di 10 ng/μL. La soluzione di plasmide di 10 ng / μL è stata diluita secondo un gradiente di 10 volte, risultando in 7 soluzioni di plasmide di 1 ng / μL, 0,1 ng / μL, 0,01 ng / μL, 1 pg / μL, 0,1 pg / μL, 0,01 pg / μL e 1 fg / μL, rispettivamente.
3.3 Preparare la soluzione di reazione Preparare come da tabella seguente.
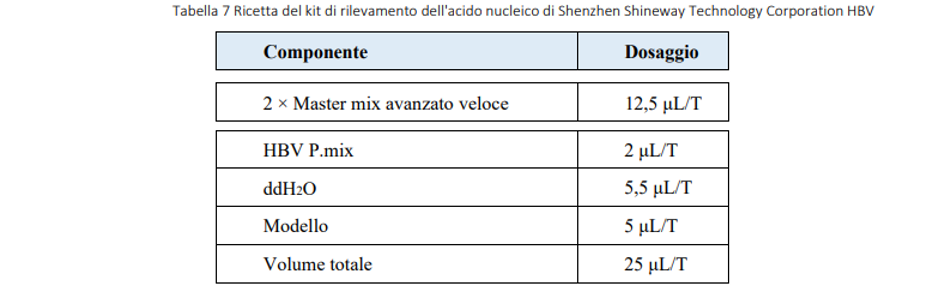
3.4 Caricare campione Secondo il processo operativo del kit di rilevamento dell’acido nucleico HBV della Shenzhen Shineway Technology Corporation, ad ogni soluzione di reazione sono stati aggiunti 5 μL di campione estratto e purificato. Dopo aver miscelato l’omogeneità, prelevare il volume corrispondente di soluzione miscelata per le reazioni della macchina in base ai diversi consumi di materiale (l’analizzatore di acido nucleico PCM SWM-01 è 2 μL/foro, il sistema di rilevamento PCR in tempo reale Bioer FQD-48A è 25 μL/provetta), sono stati eseguiti tre esperimenti paralleli ad ogni concentrazione.
3.5 Procedura di amplificazione della PCR – il sistema di rilevamento PCR in tempo reale Bioer FQD-48A : 50 ℃ , 2 min ; 95 ℃ , 15 min ; (94 ℃,15 s;55 ℃,45 s)×45cycle ;40 ℃,20 S. – Analizzatore di acido nucleico PCR SWM-01:95 ℃,3 min;(95 ℃,10 s;55 ℃,40 s) × 45 ciclo ; 40 ℃ , 20 S.
4. Risultati e analisi 4.1 Il sistema di rilevamento PCR in tempo reale Bioer FQD-48A 4.1.1 Le curve di amplificazione sono le seguenti : I risultati sono i seguenti
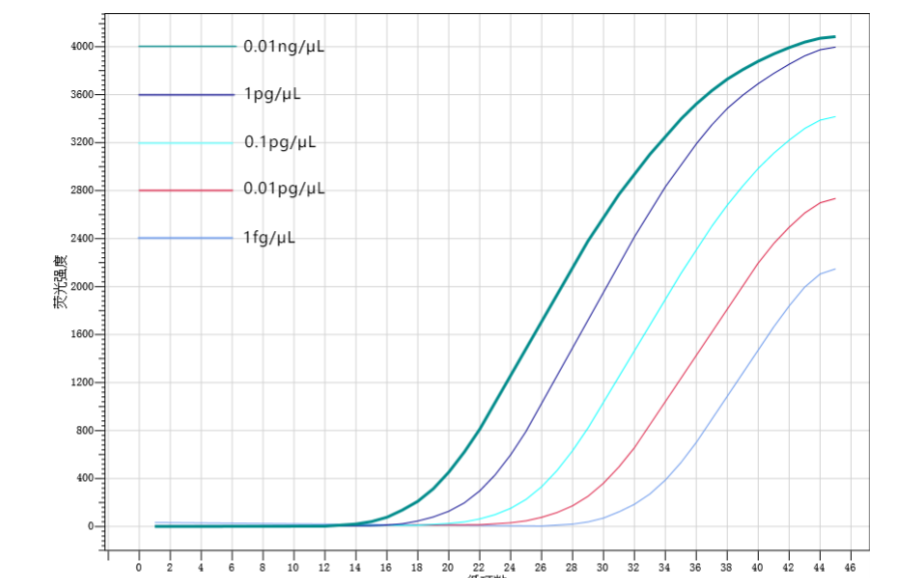
4.1.2 Risultati del valore Ct di amplificazione (Soglia predefinita di sistema)
Tabella 8 Valori Ct dei plasmidi HBV sintetizzati a diverse concentrazioni (FQD-48A da Bioer)
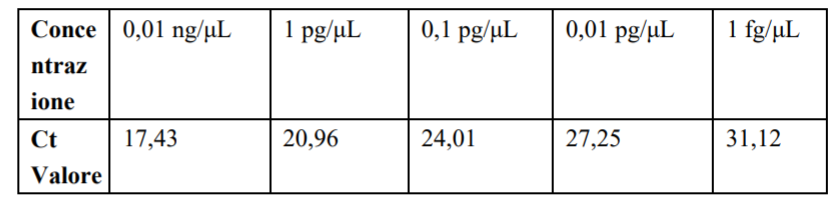
4.1.3 Analisi di correlazione lineare tra diverse concentrazioni di campioni e i loro valori CT
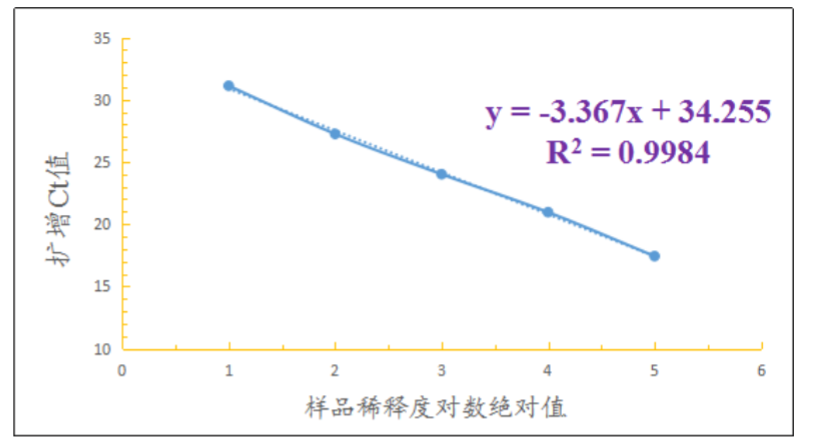
4.1.4 Analisi dei dati Come si può vedere dalla curva di amplificazione sopra, il plasmide sintetico HBV con diverse concentrazioni aveva una buona curva di amplificazione con gradiente evidente. Il limite di rilevazione stabile dei campioni di plasmide HBV era 10-8(1 fg/μL)e il valore Ct era circa 34. Il coefficiente di regressione lineare r2 del valore Ct di ciascuna concentrazione e il logaritmo della concentrazione era 0,9984, indicando che la correlazione del sistema di rilevamento della PCR in tempo reale Bioer FQD-48A del rilevamento della concentrazione del campione è buona.
4.2 Analizzatore di acido nucleico PCR SWM-01 4.2.1 Curva di amplificazione come segue :
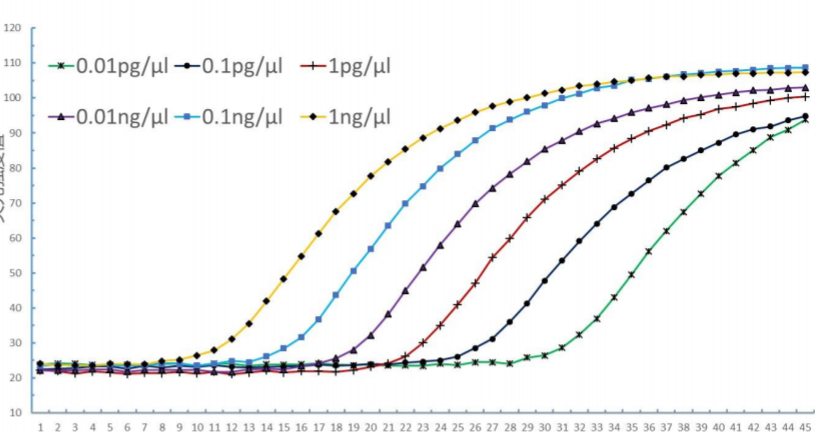
4.2.2 Risultati dei valori Ct Tabella 9 Valori Ct di plasmidi HBV sintetizzati a diverse concentrazioni (Analizzatore di acido nucleico PCR SWM-01)
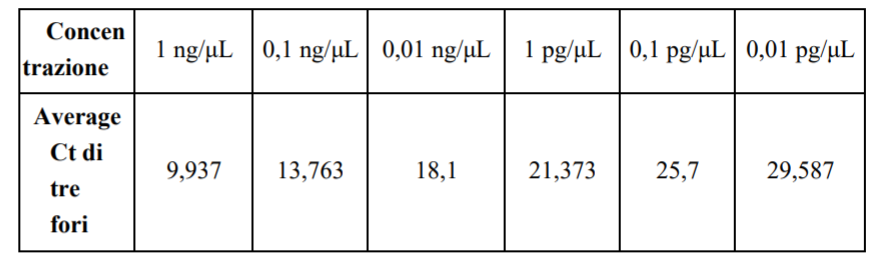
4.2.3 Analisi di correlazione lineare tra diverse concentrazioni di campioni e i loro valori
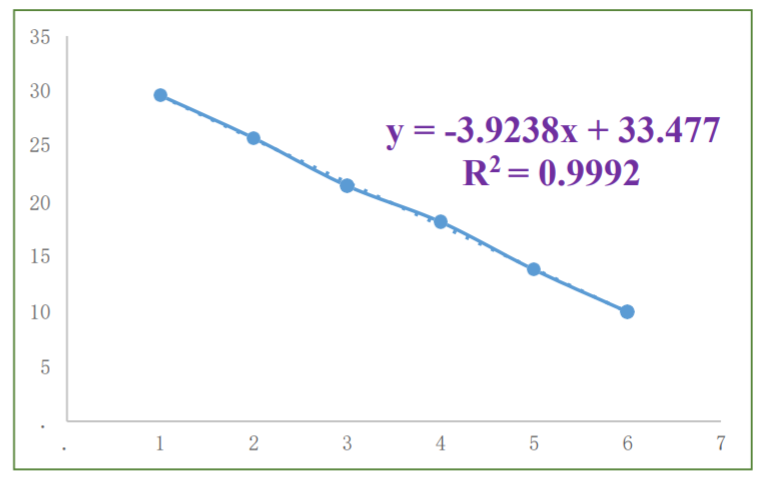
4.2.4 Analisi dei dati
Come si può vedere dalla curva di amplificazione sopra, il plasmide sintetico HBV con diverse concentrazioni aveva una buona curva di amplificazione con gradiente evidente. Il limite di rilevamento stabile dei campioni di plasmide HBV era di10-7(0,01 pg/μL o 10 fg/μL), mentre il sistema di rilevamento PCR in tempo reale Bioer FQD-48A ha un limite di rilevamento di 1 fg/μL. Il motivo principale dei diversi limiti di rilevazione è che il sistema di reazione dell’analizzatore di acido nucleico PCM SWM-01 è 2 μL, mentre il sistema di reazione del sistema di rilevazione PCR in tempo reale Bioer FQD-48A è 25 μL, il secondo è 12,5 volte il primo. Quando la concentrazione dei campioni da testare è molto bassa, l’errore di campionamento influirà sul limite di rilevamento dell’apparecchiatura. Pertanto, quando la concentrazione di campioni rari è molto bassa, le molecole di acido nucleico target potrebbero non essere aggiunte al sistema di reazione PCR durante il processo di campionamento. Il rapporto tra i sistemi di reazione tra SWM-01 e FQD-48A è di circa 1:10, e anche il rapporto dei loro limiti di rilevazione è di 1:10. Pertanto, quando il sistema di reazione di SWM-01 diventa 25 μL, il limite di rilevazione può scendere teoricamente a 1 fg/μL, in modo uguale al limite di rilevazione di FQD-48A. Tuttavia, considerando la domanda di screening qualitativo rapido clinico, nella maggior parte dei casi le concentrazioni di molecole di acido nucleico dei campioni clinici non supereranno i 10 fg/μL. L’analizzatore di acido nucleico PCR SWM – 01 è in grado di soddisfare le esigenze della diagnosi clinica in questo momento (in questo documento, l’ottava nazionale piastra standard di test dell’acido nucleico e il nono test di campioni clinici possono fornire prove). Inoltre, dopo aver soddisfatto i requisiti del limite di rilevazione dei campioni clinici, il sistema di reazione da 2 μL può migliorare significativamente la velocità del ciclo termico della PCR, ridurre significativamente i tempi di rilevazione della PCR e soddisfare i requisiti di rilevazione rapida. D’altra parte, la correlazione tra concentrazione del campione e valore Ct potrebbe riflettersi con successo in SWM-01 con 0,9891 r2 .
5. Conclusione
Quando si utilizzano lo stesso kit e campioni, la sensibilità dell’analizzatore di acido nucleico PCM SWM-01 della Shenzhen Shineway Technology Corporation è inferiore al sistema di rilevamento PCR in tempo reale Bioer FQD-48A di un ordine di grandezza. Tuttavia, considerando le differenze del sistema di reazione PCR (SWM – 01 è 2 μL, mentre FQD – 48 è 25 μL), i due hanno teoricamente la stessa sensibilità di rilevamento. L’analizzatore di acido nucleico PCR SWM-01 di Shineway può ridurre significativamente i tempi di reazione della PCR e migliorare la tempestività del rilevamento sul presupposto di soddisfare il requisito di un rapido rilevamento clinico. Allo stesso tempo, non vi era alcuna differenza significativa nel confronto lineare tra i due strumenti. Ciò indica che non vi è alcuna differenza significativa nelle prestazioni di rilevamento tra SWM-01 e FQD-48A utilizzando campioni standard di plasmidi sintetici.
2.3 Confronto delle prestazioni di SWM-01 con lo strumento commercializzato (Materiali di riferimento standard nazionali)
1. Finalità
I materiali di riferimento standard nazionali dell’acido nucleico HBV con diverse concentrazioni sono stati usati per testare i due strumenti e lo stesso campione standard e reagente di rilevazione sono stati usati per confrontare la sensibilità di rilevazione e la stabilità dei due strumenti.
2. Materiali e strumenti
1 Pechino Zhongke ispezione di qualità Biotecnology Co., Ltd
2.1 Campione di piastra standard nazionale di acido nucleico sierico del virus dell’epatite b (Approvato dal CFDA , numero di lotto 201812007) , L’acido nucleico deve essere purificato mediante estrazione di acido nucleico ; La concentrazione del campione di piastra standard nazionale (La perdita di estrazione del campione non è inclusa) è 4,6 × 10 6 UI / ml;
2.2 Kit di rilevamento dell’acido nucleico HBV Shenzhen Shineway Technology Corporation (numero di lotto 201812001);
2.3 Kit di estrazione di nutrienti a perline magnetiche Xi’an Tianlong: Contiene tutti i materiali necessari per estrazione, l’efficienza di estrazione è di circa il 4% (I dettagli dell’esperimento sono riportati nell’allegato I). Cioè, la concentrazione del campione di piastra nazionale standard di acido nucleico sierico dopo la purificazione è 1 为 1.84×10 5 IU/ml;
2.4 SWM-01 PCR Analizzatore di acido nucleico , (Certificato di registrazione dello strumento nazionale 20153400273) ;
2.5 Altri : chip di reazione, puntali di pipetta, guanti, maschere, banco (forniti dal laboratorio di medicina di laboratorio dell’ottavo ospedale affiliato, Università Sun Yat-sen).
3. Metodi
3.1 Estrazione di acido nucleico del campione HBV standard
3.1.1 Aggiungere 25 µl di microsfere magnetiche (miscelate prima dell’uso), 20 µl di proteasi K, 500 µl di soluzione di lisato e 200 µl di campioni in una provetta da centrifuga senza enzimi da 1,5 ml e fare il bagno d’acqua a 60 ℃ per 15 minuti, mescolando più volte durante il bagno;
3.1.2 Posizionare la provetta da centrifuga sulla cremagliera magnetica per 3 minuti per attirare le microsfere magnetiche nella provetta, quindi rimuovere il liquido nella provetta e rimuovere la provetta da centrifuga;
3.1.3 Aggiungere 700 µl di tampone di lavaggio A per far sospendere le microsfere magnetiche. Usare il rack magnetico per attrarre le perle magnetiche per 3 minuti, quindi rimuovere il liquido nella provetta. Tenere la provetta da centrifuga sulla griglia magnetica;
3.1.4 Aggiungere 700 µl di tampone di lavaggio B, cercare di non soffiare via le microsfere magnetiche. Usare il rack magnetico 31 per attirare le perle magnetiche e rimuovere il liquido nella provetta dopo 3 minuti, quindi rimuovere la provetta centrifuga;
3.1.5 Aggiungere 50 µl ~ 100 µl di tampone di eluizione, in modo tale da sospendere le sfere magnetiche. Prendere un bagno da 65 ℃ per 5 minuti, durante il quale agitare delicatamente la provetta per ottenere acido nucleico eluito dalle perle magnetiche ;
3.1.6 Posizionare la provetta da centrifuga sulla cremagliera magnetica per 3 minuti per attirare le microsfere magnetiche, quindi trasferire il liquido con acido nucleico in una nuova provetta da centrifuga senza nucleasi da 1,5 ml
3.1.7 Diluire il campione standard estratto ad alta concentrazione di un certo gradiente multiplo , ottenere il numero 1 ~ 7 campioni con diverse concentrazioni (1.84×10 5 IU/ml,1.84×10 4 IU/ml, 1.84×10 3 IU/ml,1.84×10 2 IU/ml,1.84×10 IU/ml ,1.84 IU/ml e 0.92×10 3 IU/m(l la perdita di campione di estrazione è inclusa ,) , conservata a -20 ℃.Campioni n. 1, n. 2 e n. 6 sono stati usati per il test di stabilità di swm-01.
3.2 Preparare la soluzione di reazione Preparare come nella tabella seguente.
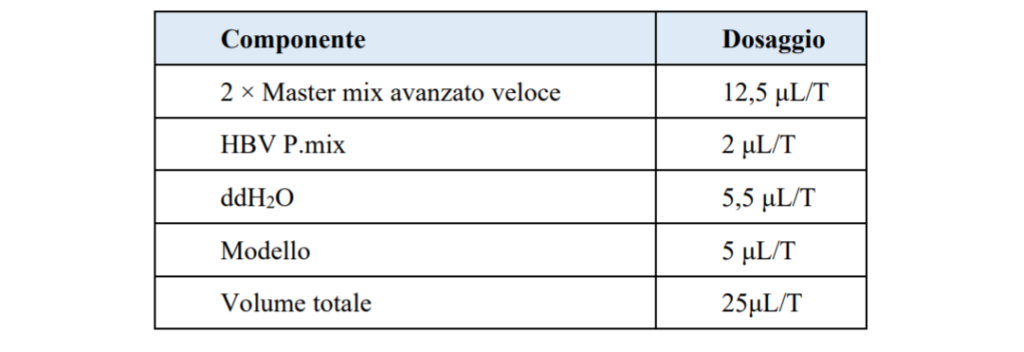
3.3Caricare campione 3.3.1 Il confronto tra sensibilità e linearità del campione tra SWM-01 e lo strumento commercializzato Secondo il processo operativo del kit di rilevamento dell’acido nucleico HBV della Shenzhen Shineway Technology Corporation, ad ogni soluzione di reazione sono stati aggiunti 5 μL di campione estratto e purificato. Dopo aver miscelato l’omogeneità, prelevare il volume corrispondente di soluzione miscelata per le reazioni della macchina in base ai diversi consumi di materiale (SWM-01 PCR Nucleic Acid Analyzer è 2 μL/foro, il sistema di 33 rilevamento PCR in tempo reale FQD-48A di Bioer è 25 μL /provetta), sono stati eseguiti tre esperimenti paralleli ad ogni concentrazione.
3.3.2 Test di stabilità dell’analizzatore di acido nucleico PCR SWM-01 Secondo il processo operativo della Shenzhen Shineway Technology Corporation HBV 34 kit di rilevazione di acido nucleico, 5 μL di campione estratto e purificato sono stati aggiunti a ciascuna soluzione di reazione. Dopo aver miscelato l’omogeneità, prelevare 2 μL/foro di soluzioni di reazione nel chip di reazione per le reazioni della macchina. Ogni concentrazione è stata ripetuta 20 volte.
3.4 Procedura di amplificazione della PCR – il sistema di rilevazione PCR in tempo reale Bioer FQD-48A : 50℃ , 2min ; 95 ℃ , 15min ; (94℃,15s;55℃,45s)×45cycle ;40℃,20S. -il PCR Analizzatore di acido nucleico SWM-01 : 95℃ , 3min ; (95 ℃ , 10s ; 55 ℃ , 40s) × 45 cicli ; 40℃ , 20S.
4. Risultati e analisi
4.1 Il sistema di rilevamento PCR in tempo reale Bioer FQD-48A 4.1.1 Le curve di amplificazione sono le seguenti : I risultati sono i seguenti :
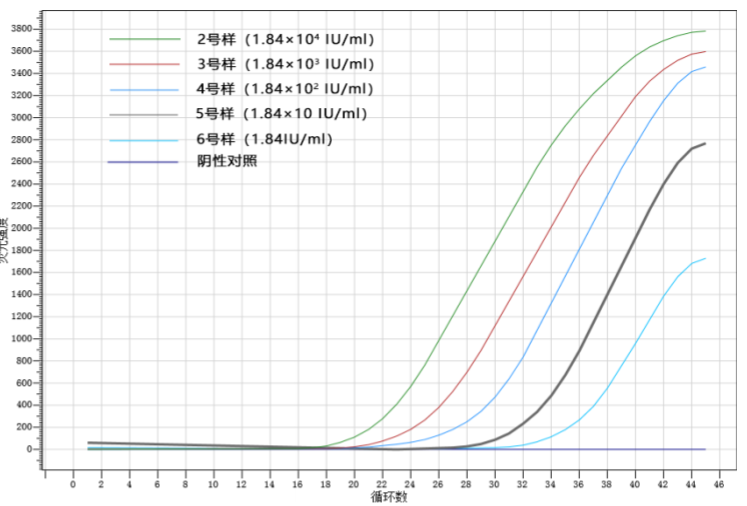
4.1.2 Risultati del valore Ct di amplificazione (Soglia predefinita di sistema)
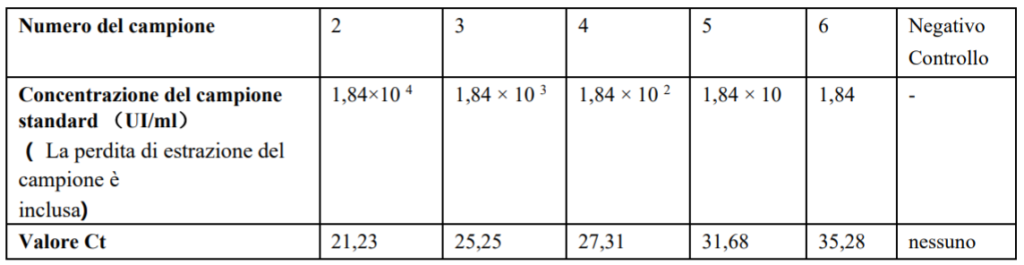
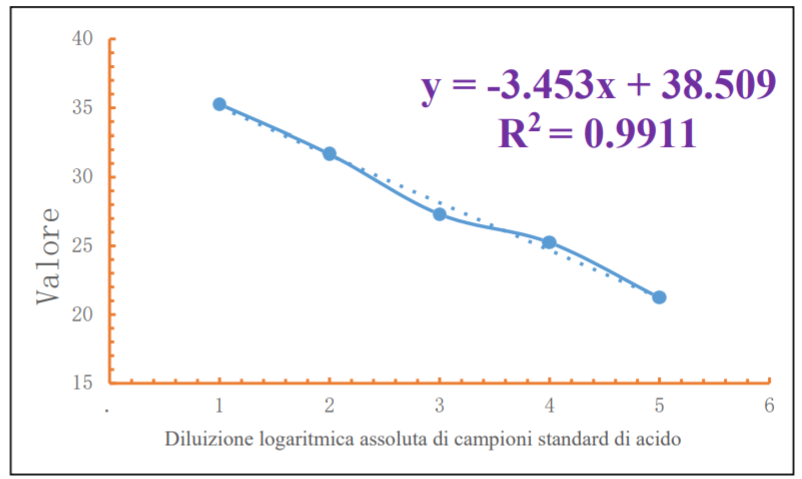
Figura 11 Analisi di correlazione lineare tra diverse concentrazioni di campione e i loro valori CT 4.1.4 Analisi dei dati (FQD-48A di Bioer)
4.1.4 Analisi dei dati
Come si può vedere dalla curva di amplificazione sopra, il plasmide sintetico HBV con diverse concentrazioni aveva una buona curva di amplificazione con gradiente evidente. Se la perdita di estrazione non è inclusa, lo strumento ha un limite di rilevazione stabile di 46 UI / ml (la diluizione standard del campione è10-5) ; Il coefficiente di regressione lineare r2 del valore Ct di ciascuna concentrazione e il logaritmo della concentrazione era 0.9911, indicando che la correlazione del Bioer in tempo reale Il sistema di rilevamento PCR FQD-48A del rilevamento della concentrazione del campione è buono. Secondo il risultato dell’esperimento del kit di estrazione dei nutrienti di Tianlong Magnetic Beads, l’efficienza di estrazione del kit è di circa il 4% (i risultati della validazione Diluizione logaritmica assoluta di campioni standard di acido nucleico HBV . 1 2 3 4 5 6 15 20 25 30 y = -3.453x + 38.509 R2 = 0.9911 35 40 Valore Ct 36 si trovano nell’appendice a, “esperimento di verifica dell’efficienza di estrazione dell’acido nucleico dei nutrienti di Tianlong Magnetic Beads 37 Kit di estrazione “). Se viene inclusa l’efficienza di estrazione, dopo l’estrazione, la concentrazione effettiva di concentrazioni diluite di 46 UI/ml di materiale standard nel siero HBV è circa 1,84 UI/ml, quindi il limite di rilevazione del sistema di rilevazione PCR in tempo reale BioQ FQD-48A è 1,84 UI/ml.
4.2 Analizzatore di acido nucleico PCR SWM-01 4.2.1 Curva di amplificazione come segue :
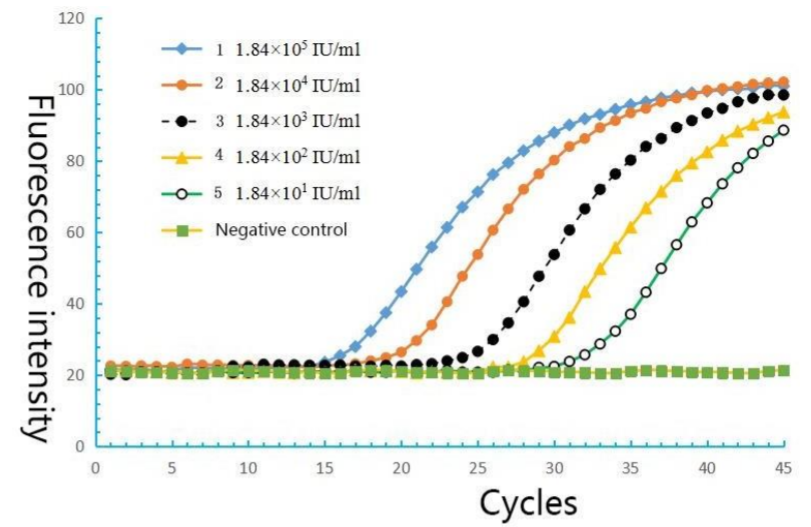
4.2.2 Risultati dei valori Ct
Tabella 12 Valori Ct di campioni standard di HBV a diverse concentrazioni (Analizzatore di acido nucleico PCR SWM-01)
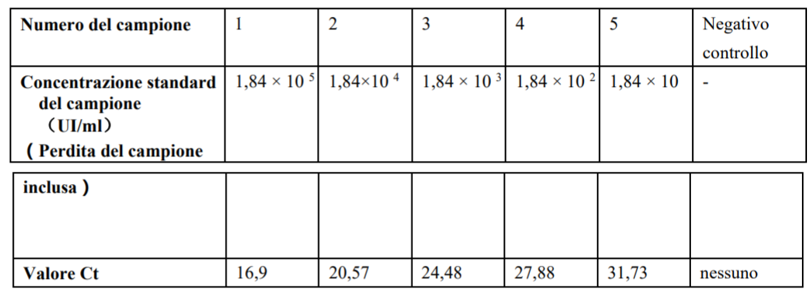
4.2.3 Analisi di correlazione lineare tra diverse concentrazioni di campioni e i loro valori CT
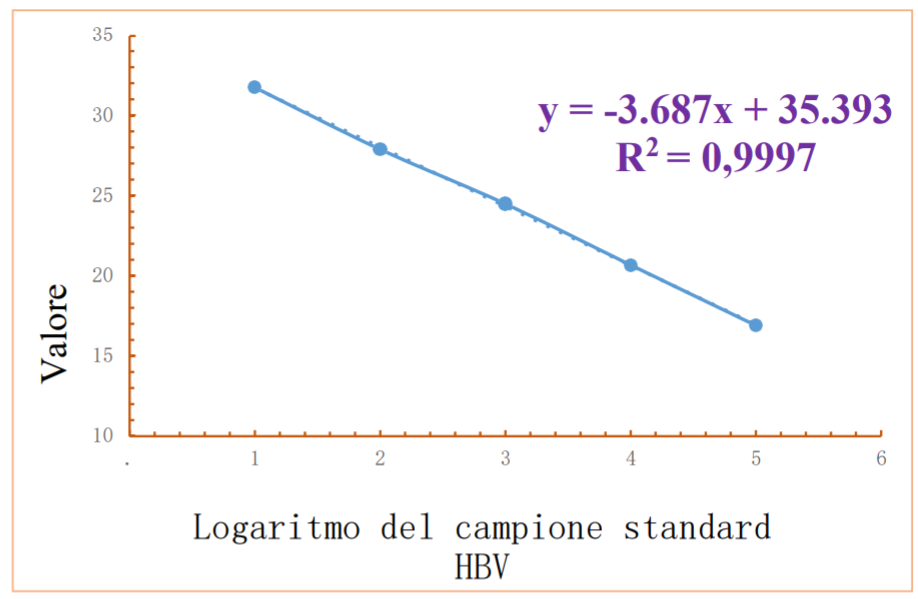
4.2.4 Analisi dei dati
Come si può vedere dalla curva di amplificazione sopra, il plasmide sintetico HBV con diverse concentrazioni aveva una buona curva di amplificazione con gradiente evidente. Se la perdita di estrazione non è inclusa, lo strumento ha un limite di rilevazione stabile di 460 UI/ml (la diluizione standard del campione è 10-4 , circa 460 IU/ml). Secondo il risultato dell’esperimento del kit di estrazione di nutrienti perline magnetiche Tianlong, l’efficienza di estrazione del kit è di circa il 4% (convalida risultati vedere l’appendice a, “esperimento di verifica dell’efficienza di estrazione dell’acido nucleico del kit di estrazione del nutriente perline magnetiche Tianlong”). Se l’efficienza di estrazione è inclusa, dopo l’estrazione, la concentrazione effettiva di concentrazioni diluite di 460 UI/ml di materiale standard nel siero HBV è di circa 18,4 UI/ml, quindi il limite di rilevazione dell’analizzatore di acido nucleico PCR SWM-01 è 18,4 UI/ml. La sensibilità dell’analizzatore di acido nucleico PCR SWM-01 della Shenzhen Logaritmo del campione standard HBV diluzione . 1 2 3 4 5 6 10 15 20 25 y = -3.687x + 35.393 R2 = 0,9997 30 35 Valore Ct 40 Shineway Technology Corporation è inferiore al sistema di rilevamento PCR in tempo reale Bioer FQD-48A di 41 un ordine di grandezza. Ancora una volta, riteniamo che ciò sia dovuto alle differenze tra i sistemi di reazione PCR. (SWM-01 è 2 μL , mentre FQD-48 è 25 μL). Se SWM-01 ha un sistema di reazione di 25 μL , avrà teoricamente lo stesso limite di rilevazione di FQD48A. Ma considerando la domanda di screening qualitativo rapido clinico, nella maggior parte dei casi le concentrazioni di molecola di acido nucleico dei campioni clinici non supererà i 18,4 UI/ml, l’analizzatore di acido nucleico PCR SWM – 01 può soddisfare le esigenze della diagnosi clinica in questo momento (in questo documento, il nono test dei campioni clinici può fornire prove). Inoltre, dopo aver soddisfatto i requisiti del limite di rilevazione dei campioni clinici, il sistema di reazione da 2 μL può migliorare significativamente la velocità del ciclo termico della PCR, ridurre significativamente i tempi di rilevazione della PCR e soddisfare i requisiti di rilevazione rapida. D’altra parte, il coefficiente di regressione lineare r2 del valore Ct di ciascuna concentrazione e il logaritmo della concentrazione era 0.9947 , indicando che la correlazione dell’analizzatore di acido nucleico PCM SWM-01 del rilevamento della concentrazione del campione è buona.
4.3 Test di stabilità dell’analizzatore di acido nucleico PCR SWM-01
4.3.1 Risultati del valore di amplificazione Ct
Tabella 13 Tabella statistica dei valori Ct dell’analizzatore di amplificazione dell’acido nucleico swm-01 nel test di stabilità
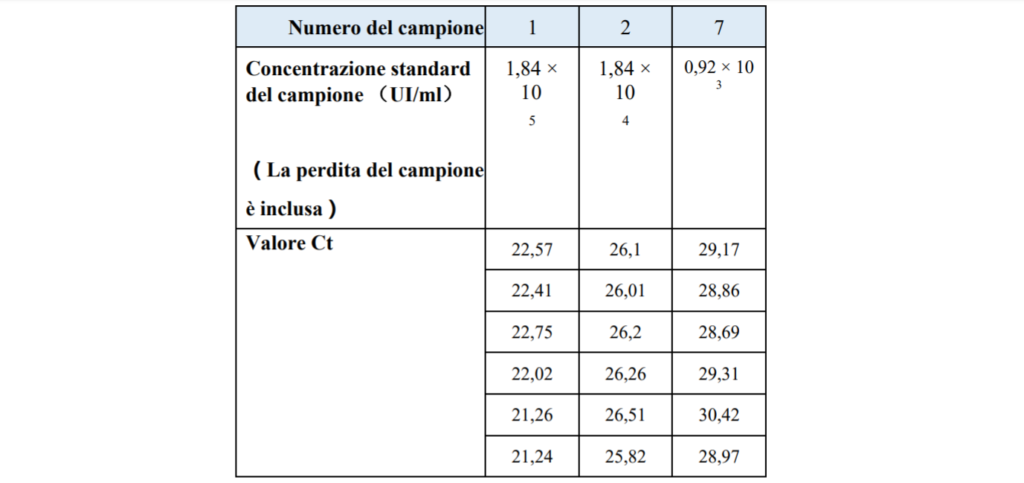
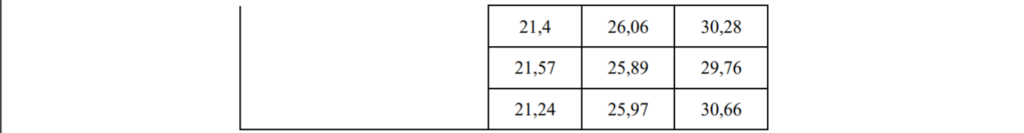
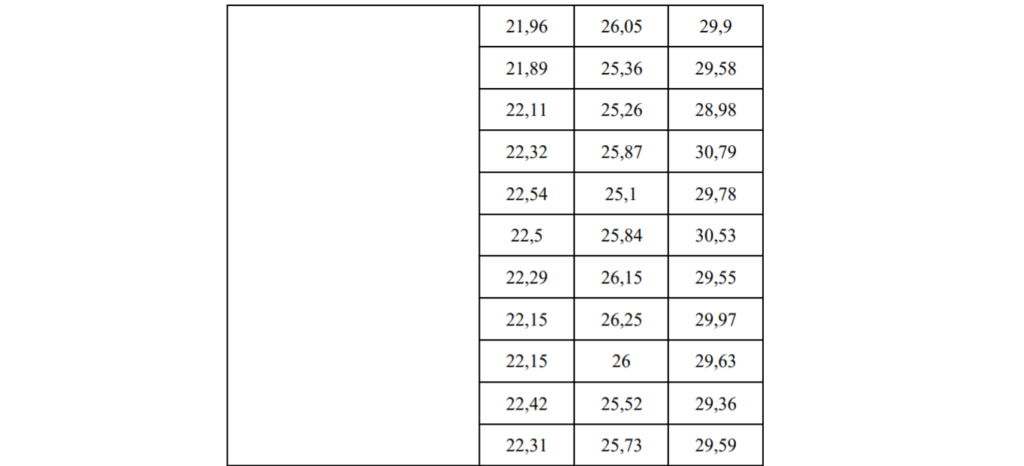
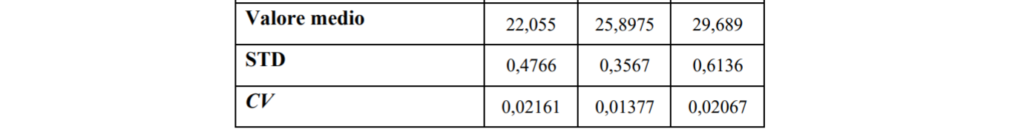
4.3.2 Curva di amplificazione Di seguito sono stati mostrati solo i risultati di un chip di reazione.
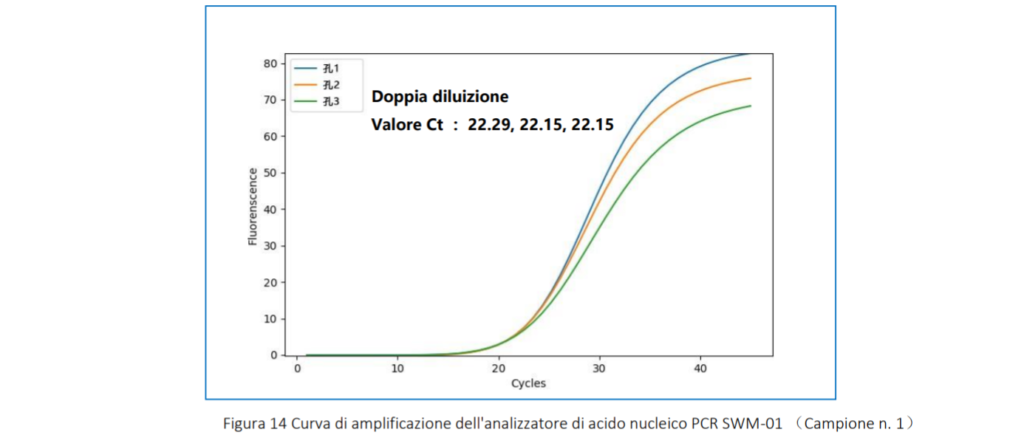
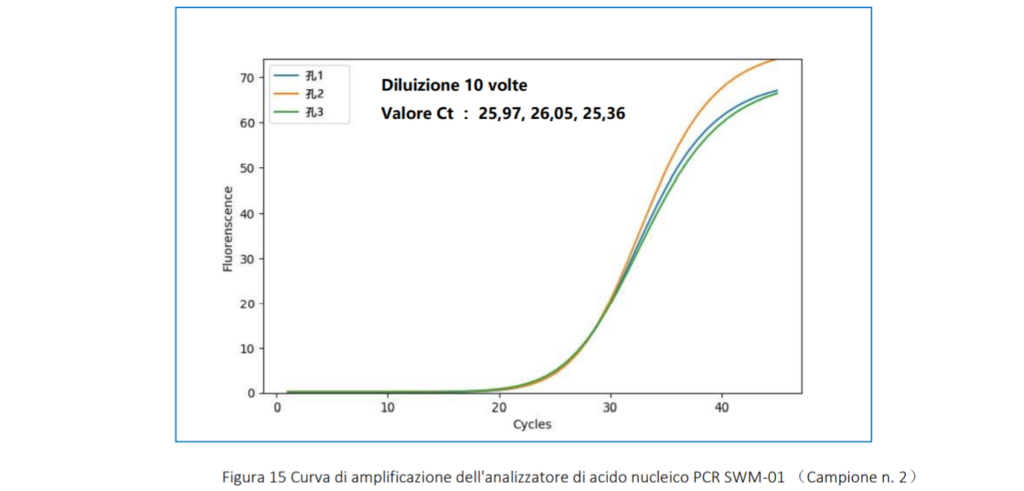
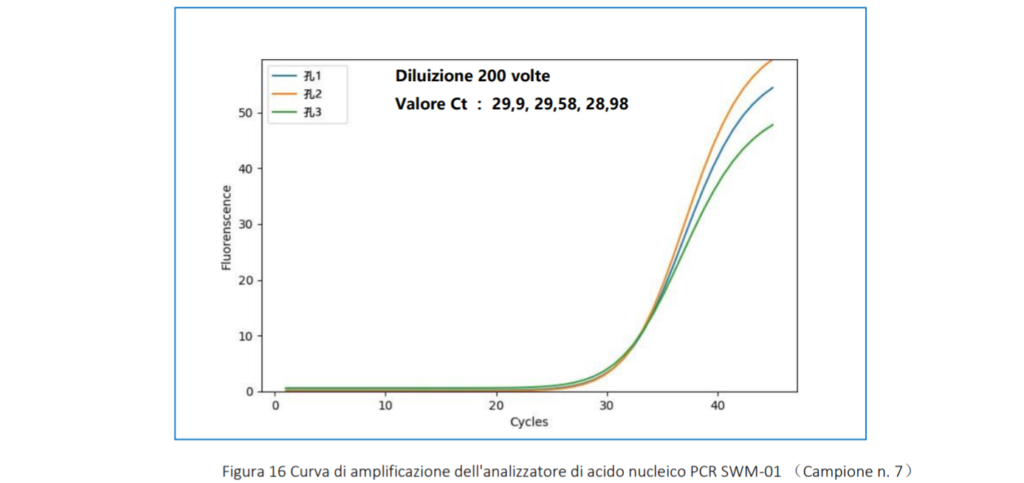
4.3.3 Analisi dei dati
Come si può vedere dalla curva di amplificazione sopra, il plasmide sintetico HBV con diverse concentrazioni aveva una buona curva di amplificazione con gradiente evidente. La CV Diluizione 10 volte Valore Ct : 25,97, 26,05, 25,36 45 dei valori Ct di alta concentrazione, media concentrazione e bassa concentrazione sono : 2,16%, 1,38% , 2,07%.Il CV è inferiore al 3% , indica che swm-01 ha una buona stabilità nel rilevare diverse concentrazioni di campione.
5. Conclusione
Quando si utilizzano lo stesso kit e campioni, la sensibilità dell’analizzatore di acido nucleico PCM SWM-01 della Shenzhen Shineway Technology Corporation è inferiore al sistema di rilevamento PCR in tempo reale Bioer FQD-48A di un ordine di grandezza. Tuttavia, considerando le differenze del sistema di reazione PCR (SWM – 01 è 2 μL, mentre FQD – 48 è 25 μL), i due dispositivi sopra citati hanno teoricamente la stessa sensibilità di rilevamento. L’analizzatore di acido nucleico PCR SWM-01 della Shenzhen Shineway Technology Corporation è in grado di ridurre significativamente i tempi di reazione della PCR e migliorare la tempestività del rilevamento sulla base del requisito della rapida rilevazione clinica (qualitativa) ; Allo stesso tempo, non c’era alcuna differenza significativa nel confronto lineare tra i due strumenti. Questo indica che non vi è alcuna differenza significativa nelle prestazioni di rilevamento tra SWM-01 e FQD48A utilizzando campioni standard nazionali. Campione di siero standard HBV nazionale con tre concentrazioni alta, media e bassa sono stati usati come campione di acido nucleico. Ogni concentrazione è stata testata 20 volte utilizzando l’analizzatore di acido nucleico PCM SWM-01 della Shenzhen Shineway Technology Corporation. Dopo un’analisi statistica dei valori Ct, si è concluso che i coefficienti di variazione del valore Ct dell’SWM-01 della Shenzhen Shineway Technology Corporation erano rispettivamente del 2,16%, 1,38% e 2,07% (tutti meno del 3%). I risultati hanno mostrato che SWM-01 era in linea con gli standard tecnici pertinenti e aveva una buona stabilità per il rilevamento di diverse concentrazioni di campioni.
2.4 Confronto con gli strumenti elencati (campioni clinici)
1. Finalità
Utilizzando lo stesso reagente PCR, sono stati utilizzati lo strumento PCM in tempo reale SWM-01 e Roche 480 (strumento di riferimento) per confrontare la coerenza dei risultati dei test, a dimostrazione del fatto che 47 il nostro prodotto ha le stesse prestazioni di rilevamento dei campioni clinici.
2. Materiali e strumenti
2.1 Strumenti Strumento di acquisizione dati 34970A Agilent, sensore di temperatura dedicato
2.1.1 Analizzatore di acido nucleico PCR SWM-01
2.1.2 Roche Diagnostics GmbH – Strumento PCR in tempo reale, LightCycler 480 (National Machinery Note 20163402935)
2.1.3 Centrifuga palmo, micro pipetta, ecc.
2.2 Materiali
2.2.1 Kit di rilevamento dell’acido nucleico HBV Shenzhen Shineway Technology Corporation (numero di lotto 201812001)
2.2.2 Campione Campioni di siero clinico HBV dell’ottavo ospedale affiliato dell’Università di Sun Yat-sen, la dimensione del campione è 125, numero campione 1-125.
2.2.3 Kit di estrazione di nutrienti a perline magnetiche Xi’an Tianlong
3. Metodo
3.1 Estrazione di acido nucleico
3.1.1 Aggiungere 25 μl di microsfere magnetiche (miscelate prima dell’uso), 20 μl di proteinasi K, 500 μl di lisato e 200 μl di campione in una provetta da centrifuga senza enzimi da 1,5 ml e fare il bagno per 60 minuti a 60 ° C per diversi minuti;
3.1.2 Posizionare la provetta da centrifuga sul supporto magnetico per 3 minuti, in modo che le microsfere magnetiche nella provetta siano assorbite, rimuovere il liquido nella provetta e rimuovere la provetta da centrifuga;
3.1.3 Aggiungere 700 ml di soluzione di lavaggio A e utilizzare la cornice magnetica per adsorbire le perle magnetiche. Dopo 3 minuti, rimuovere il liquido nella provetta e mantenere la centrifuga sulla griglia magnetica della provetta;
3.1.4 Aggiungere 700 ml di soluzione di lavaggio B, cercare di non soffiare via le microsfere magnetiche, utilizzare una griglia magnetica per adsorbire le microsfere magnetiche, rimuovere il liquido nella provetta dopo 3 minuti e rimuovere la provetta da centrifuga;
3.1.5 Aggiungere 50 μl ~ 100 μl di eluente, risospendere le microsfere magnetiche e bagnare a 65 ° C per 48 5 minuti, agitando delicatamente per diluire l’acido nucleico dalle perle magnetiche;
3.1.6 Posizionare la provetta da centrifuga sulla griglia magnetica per 3 minuti per adsorbire le sfere magnetiche. Trasferire il liquido in una nuova provetta da centrifuga priva di nucleasi da 1,5 ml e conservare a -20 ° C. 3.2 Preparazione della soluzione di reazione
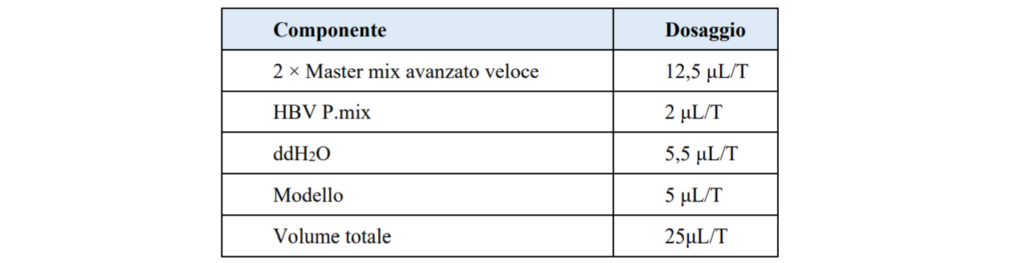
3.3 Campione misto
Secondo la procedura operativa del kit di rilevamento dell’acido nucleico HBV, 5 μL di campione purificato vengono aggiunti a ciascuna soluzione di reazione. Dopo la miscelazione. La quantità di caricamento della soluzione mista si basa sulla capacità di campionamento di diversi strumenti. (2 μL/pozzetto per PCR Analizzatore di acido nucleico SWM-01 e 25 μL/provetta per la macchina per PCR Roche 480 in tempo reale).
3.4 Procedura di reazione di amplificazione – Macchina per PCR in tempo reale Roche:50℃,2min;95℃,15min;(94℃,15s;55℃, 45s)×45 ciclo;40℃,20S. – Analizzatore di acido nucleico SWM01:95℃,3min;(95℃,10s;55℃,40s)×45cycle ; 40℃,20S.
3.5 Analisi dei dati Il metodo di valutazione della coerenza KAPPA viene utilizzato per statistiche e analisi. 4. Risultati e analisi Secondo il metodo di test di coerenza KAPPA, la consistenza dello strumento sperimentale e dello strumento di riferimento è la più forte.
Richiedi il report completo ….
CONTATTI
Marco Brecciaroli (Dir. Marketing) Tel. +39 335 5611710
Email: marco@simitecno.it